Moleculaire stoffen
Alles wat je om je heen ziet, bestaat uit moleculen.
Alle moleculen hebben bepaalde eigenschappen. Moleculen kunnen samen moleculaire stoffen vormen.
Wil je precies weten wat de eigenschappen van moleculaire stoffen zijn? Lees dan snel verder, want Mr. Chadd gaat het je uitleggen!
In deze samenvatting vind je:
-
- Geleidingsvermogen en naamgeving
- Atoombindingen
- Vanderwaalsbindingen
- Mengsels van moleculaire stoffen
1.1: Geleidingsvermogen en naamgeving
Moleculaire stoffen bestaan uit moleculen. Dat zijn kleine deeltjes zonder lading die uit atomen bestaan. Omdat ze geen lading hebben, geleiden ze geen stroom. Als de atomen in een molecuul hetzelfde zijn, dan heet de stof een element. Als het twee verschillende atomen zijn, dan noem je dit een verbinding.
Als je naar de formule van een stof kijkt, dan kun je zien of het om een moleculaire stof gaat. Een moleculaire stof bestaat namelijk alleen uit niet-metalen. Ze geleiden dus geen stroom, omdat ze alleen uit niet-metalen bestaat. Of je met een metaal of niet-metaal te maken hebt, kun je aflezen in het periodiek systeem .
Een stof kan stroom geleiden als het molecuul aan twee eisen voldoet. Hij moet bestaan uit geladen deeltjes en de geladen deeltjes moeten vrij kunnen bewegen. De geladen deeltjes in een molecuul noem je ionen. Het gaat dan dus niet om een moleculaire stof, maar om een ion of een zout .
Je kunt de naam van een moleculaire stof vinden door een aantal stappen te doen. Je moet eerst weten hoe vaak ieder atoom voorkomt in de stof. Dit kun je zien aan de kleine getallen rechtsonder elk atoom. NH3 bestaat bijvoorbeeld uit 1 N-atoom (stikstof) en 3 H-atomen (waterstof). Je kunt in de naam aangeven hoe vaak ze voorkomen met bepaalde voorvoegsels. Deze kun je vinden in tabel 66C van je Binas.
Veel stoffen hebben een triviale naam en een systematische naam. De triviale naam is wat er door veel mensen gebruikt wordt dus bijvoorbeeld ‘water’ voor H2O. De systematische naam is de officiële naam. De officiële naam voor water is “diwaterstofmono-oxide”. De triviale en systematische namen van stoffen kun je vinden in tabel 66A van je Binas.
Zo werkt de app
1.2: Atoombindingen
Moleculen bestaan uit twee of meerdere atomen. De binding tussen die twee atomen noemen we ook wel een atoombinding. Deze binding bestaat doordat er van beide atomen één elektron zich bindt aan het elektron van het andere atoom. Deze elektronen heten bindingselektronen.
Deze verbinding tussen beide elektronen ligt soms in het midden. Dit is bijvoorbeeld het geval bij een binding tussen twee dezelfde atomen of bij een binding tussen en C-atoom en een H-atoom. Het kan ook zo zijn dat de bindingselektronen dichter bij het ene atoom zitten dan bij het andere atoom. Dit noemen we een polaire atoombinding . Deze vind je bijvoorbeeld tussen een O-atoom en een H-atoom of een N-atoom en een H-atoom.
Structuurformules van een molecuul geven aan hoe atomen in een bepaald molecuul aan elkaar zijn verbonden. Hieronder zie je de structuurformule van water. De streepjes tussen de atomen zijn atoombindingen. De covalentie van een atoom zegt iets over het aantal bindingen dat een bepaald atoom kan maken. De covalentie van waterstof is bijvoorbeeld 1 en de covalentie van koolstof is 4. Dat betekent dat waterstof altijd 1 binding met een ander atoom moet aangaan en koolstof altijd 4.
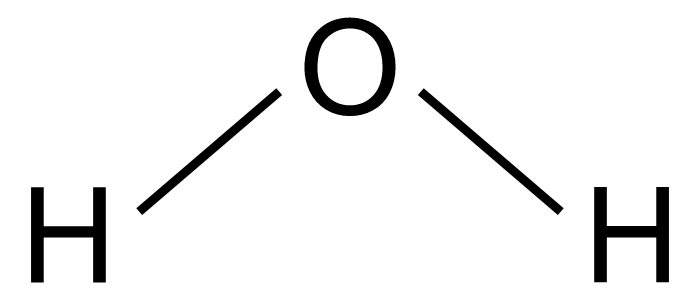
Dit kunnen ook meervoudige bindingen zijn. Dit gebeurt als er meer dan één binding tussen twee atomen bestaat. Bij etheen (zie het plaatje hieronder) is er bijvoorbeeld een dubbele binding tussen de twee C-atomen. Atoombindingen zijn heel sterk en kunnen alleen kapot gaan als er een bepaalde chemische reactie plaatsvindt waarbij de bindingen los van elkaar komen te zitten.
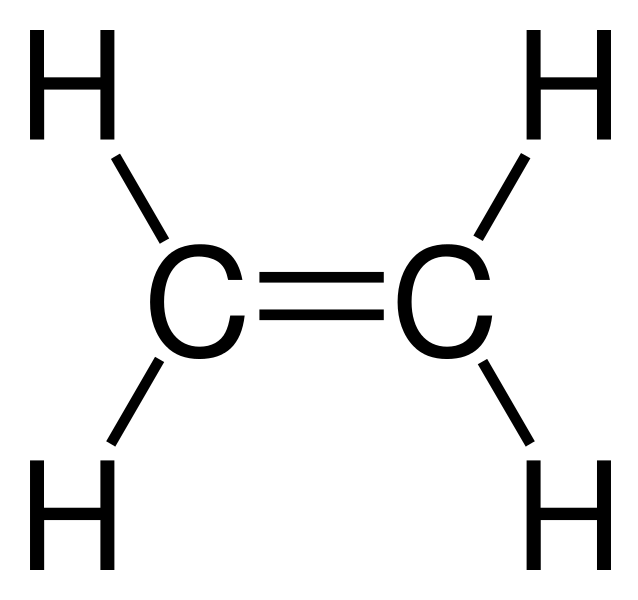
1.3: Vanderwaalsbindingen
Alle stoffen hebben drie verschillende fases: vast (s), vloeistof (l) en gas (g). Onder het smeltpunt is een stof vast, bij water is dit bijvoorbeeld ijs. Tussen het smeltpunt en het kookpunt is de stof een vloeistof, dit is water zoals het uit de kraan komt. Boven het kookpunt is het een gas, dit noemen we bij water waterdamp. De moleculen van een stof veranderen niet als de fase verandert. De overgangen tussen verschillende fasen hebben verschillende namen:
- Van gas naar vloeistof: condenseren
- Van vloeistof naar gas: verdampen
- Van vaste stof naar vloeistof: smelten
- Van vloeistof naar vaste stof: stollen
- Van vaste stof naar gas: sublimeren
- Van gas naar vaste stof: rijpen
In de vaste fase zijn moleculen regelmatig gerangschikt. Ze blijven dan op hun plaats staan en trillen rond een vast punt. In de vloeibare fase zijn de moleculen niet meer regelmatig gerangschikt. Ze blijven dicht bij elkaar, maar hebben nu wel meer ruimte om te bewegen. In de gasvormige fase zit er veel meer ruimte tussen de moleculen. Ze bewegen dan ook veel sneller. Tussen de verschillende moleculen is er lege ruimte. Hierin zit ‘niets’.
Vanderwaalsbindingen zijn bindingen die tussen moleculen voorkomen. Deze komen alleen voor in de vloeibare fase en in de vaste fase van een stof. Hij komt niet voor in de gasfase van moleculen omdat de afstand tussen de verschillende moleculen dan te groot is. De bindingen breken dus als de stof warmer wordt. Als alle bindingen verbroken zijn, dan heeft de stof het kookpunt bereikt.
Hoe sterker de vanderwaalsbinding tussen twee moleculen is, hoe hoger het kookpunt is van die stof. Het kost dan meer moeite om de bindingen te verbreken, dus is daar meer energie en dus warmte voor nodig. De vanderwaalsbindingen tussen zwaardere moleculen is sterker. Grote en zware moleculen hebben dus een hoger kookpunt.
1.4: Mengsels van moleculaire stoffen
Stoffen die goed oplossen in water hebben vaak een bepaalde groep in de structuurformule. Er komt namelijk meestal een OH-groep of een NH-groep voor in de moleculen. Deze groepen kunnen goed waterstofbruggen vormen met water. Door de waterstofbruggen kunnen de stoffen goed worden opgelost in water. Zulke stoffen noem je ook wel hydrofiel . Dit betekent letterlijk “houdt van water”. Stoffen die niet goed oplossen in water noem je hydrofoob. Dit betekent “is bang voor water”.
Moleculen met een OH-groep lossen meestal goed op in water. Soms heb je moleculen waarbij er veel C-atomen aanwezig zijn en weinig OH-groepen. De oplosbaarheid van die stof is dan een stuk lager dan wanneer er veel OH-groepen en weinig C-atomen aanwezig zijn. Je kunt laten zien dat een bepaalde stof opgelost is door er (aq) achter te zetten in plaats van de fase.
De oplosbaarheid van een bepaalde stof zegt iets over hoeveel gram van een bepaalde stof er in honderd gram water opgelost kan worden. De oplosbaarheid wordt vaak beïnvloed door de temperatuur van het water. Voor vaste stoffen geldt vaak dat hoe hoger de temperatuur is, hoe meer vaste stof er opgelost kan worden in het water. Voor gassen geldt juist dat hoe hoger de temperatuur is, hoe minder gas er opgelost kan worden in het water. Bij elke temperatuur kun je een maximaal aantal gram stof oplossen in honderd gram. Als er minder dan dit aantal wordt opgelost, dan heet dit een onverzadigde oplossing. Als deze hoeveelheid precies wordt toegevoegd, dan wordt dit een verzadigde oplossing genoemd. Als je dan nog meer stof toevoegt, dan blijft deze op de bodem liggen of drijven op het water.
Moleculaire stoffen mengen goed met elkaar als ze of allebei hydrofiel zijn of allebei hydrofoob. Als er een hydrofiele stof is en een hydrofobe stof dan mengt dit niet goed. Dit is bijvoorbeeld het geval bij olie en water. Als je deze stoffen met elkaar probeert te mengen dan ontstaan er twee verschillende lagen. Door het toevoegen van een emulgator, kunnen een hydrofiele stof en een hydrofobe toch met elkaar gemengd worden.
Bij twee hydrofiele of twee hydrofobe stoffen ontstaat er vaak een oplossing. Dit is een mengsel waarbij beide stoffen zich door elkaar heen bevinden. Oplossingen zijn altijd helder. Bij twee verschillende stoffen kunnen er verschillende mengsels ontstaan. Deze mengsels zijn troebel.
- Nevel: mengsel van een gas en een vloeistof. Hierbij zweven er kleine druppeltjes vloeistof in een gas.
- Suspensie: mengsel van een vaste stof met een vloeistof. Er zweven dan kleine deeltjes van de vaste stof in de vloeistof.
- Schuim : mengsel van een gas en een vloeistof. Er zweven belletjes gas in een vloeistof.
- Emulsie: mengsel van twee verschillende vloeistoffen. Hierbij zweven er druppeltjes van de ene vloeistof in de andere.
- Rook: mengsel van een vaste stof in een gas. Er zitten dan kleine deeltjes van de vaste stof in het gas.
Werkt u in het vo of mbo? Plan direct een vrijblijvende demonstratie in!
We laten u graag geheel vrijblijvend zien hoe Mr. Chadd werkt, hoe het kan worden ingezet en wat de meerwaarde is. Dit doen we in een fysieke of online afspraak van zo'n 30 minuten. Let op! Deze demonstratie is alleen bedoeld voor mensen die werkzaam zijn in het vo of mbo, NIET voor leerlingen!

Meer informatie over Mr. Chadd
Laat hieronder uw gegevens achter en we sturen u geheel vrijblijvend meer informatie over Mr. Chadd op!

Werkt u in het vo of mbo? Neem contact op!
Bent u benieuwd naar de voordelen van Mr. Chadd of heeft u andere vragen? Laat uw gegevens achter en wij nemen zo snel mogelijk contact op.

