Atoombouw
Atoombouw
Een atoom is opgebouwd uit een positieve atoomkern bestaande uit protonen en neutronen met daaromheen een negatieve wolk van elektronen.
Een atoom heeft een lading. Deze lading komt doordat protonen die in de kern zijn positief zijn en de elektronen negatief. Deze samen opgeteld geeft de lading van de atoom weer. Neutronen hebben echter geen lading, deze worden neutraal genoemd. Wanneer een atoom geen lading heeft (wanneer het atoom dus geen ion is), is de lading van de elektronenwolk precies even groot als die van de atoomkern.
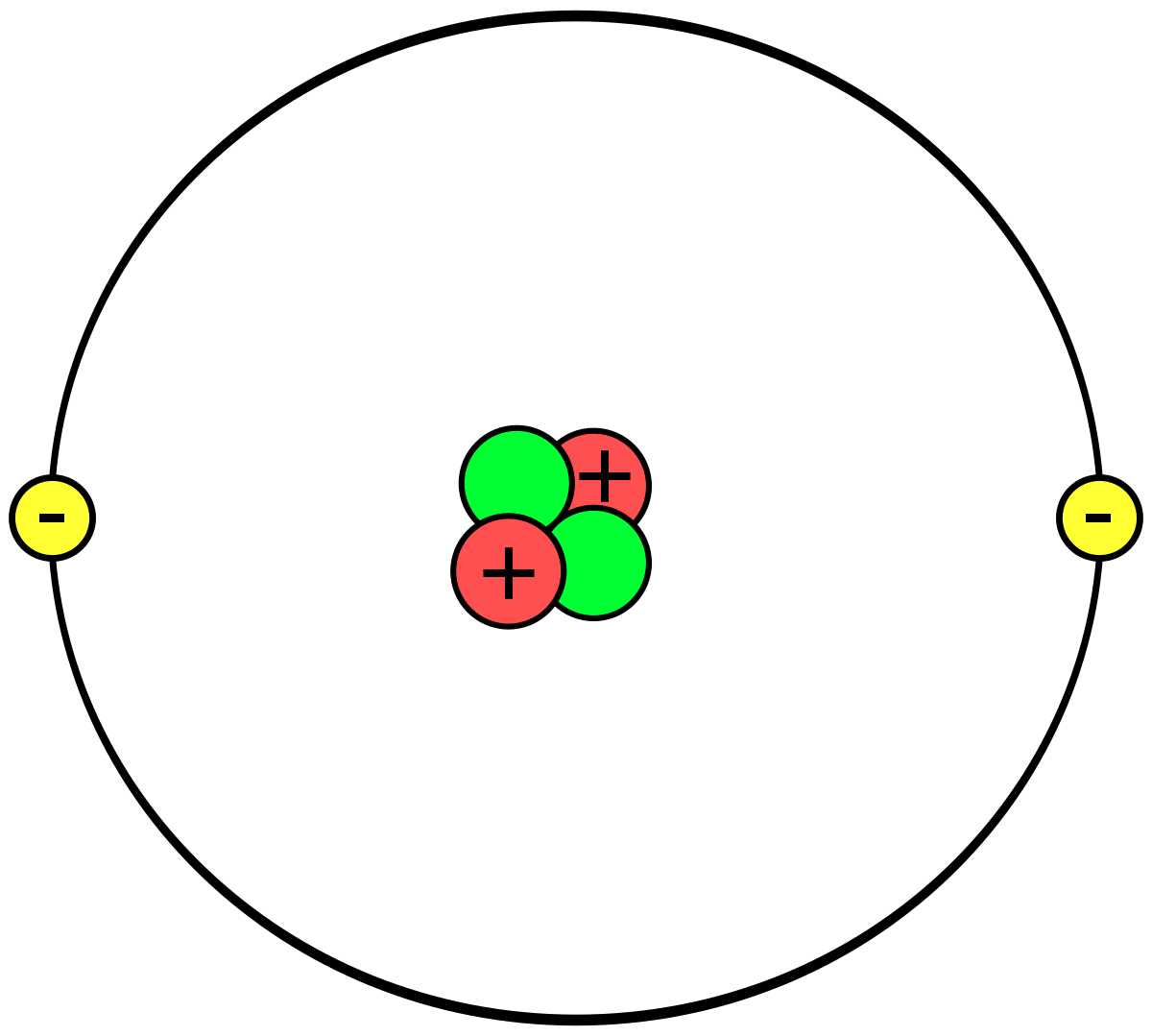
Protonen (rode deeltjes)
Protonen zijn positief geladen deeltjes. Het aantal protonen bepaalt de atoomsoort. Kwik heeft atoomnummer 80 en heeft ook 80 protonen in de kern. Thallium heeft atoomnummer 81 en heeft 81 protonen in de kern. Per atoomsoort staat dus vast hoeveel protonen er in de kern zitten. Wanneer er een proton in of uit de kern gaat (dit kan gebeuren door straling), verandert de atoomsoort dus als geheel.

Neutronen (groene deeltjes)
Neutronen zijn neutraal geladen deeltjes. Per atoomsoort staat niet van tevoren vast hoeveel neutronen er in de kern aanwezig zijn. Wanneer twee atomen van dezelfde soort een verschillend aantal neutronen hebben, zijn het isotopen van elkaar. Zo heeft Kwik zeven stabiele isotopen: 196Hg, 198Hg, 199Hg, 200Hg, 201Hg, 202Hg en 204Hg. Het getal dat voor de atoomsoort Hg staat, is het massagetal. Het massagetal is de optelsom van het aantal protonen en neutronen in de kern. Gezien het aantal protonen altijd gelijk is bij Kwik (80), kun je uitrekenen dat Kwik stabiele isotopen heeft met 116, 118, 119, 120, 121, 122 en 124 neutronen in de kern.
Elektronen (gele deeltjes)
Elektronen zijn negatief geladen deeltjes. Elektronen zijn veel lichter dan neutronen en protonen, de massa van een elektron is zelfs zo klein dat deze te verwaarlozen is. De elektronen zweven in schillen rond de kern van het atoom. Niet alle schillen bevatten evenveel elektronen. De elektronen in de buitenste schil zijn het belangrijkst. Deze elektronen zijn namelijk betrokken bij het vormen en verbreken van chemische bindingen tussen atomen. De elektronen in de buitenste schil worden ook wel de valentie-elektronen genoemd.
Het nummer van de periode in het periodiek systeem komt overeen met het aantal schillen dat bij dat atoom in gebruik is. In schil 1 kunnen maximaal 2 elektronen, in schil 2 kunnen maximaal 8 elektronen, in schil 3 kunnen maximaal 18 elektronen en in schil 4 kunnen maximaal 32 elektronen. De verschillende schillen worden vaak aangeduid als K, L, M en N-schillen. Aan de groep in het periodiek systeem is het aantal valentie-elektronen af te lezen. Alle atomen uit groep 1 van het periodiek systeem hebben dus één valentie-elektron en alle atomen uit groep 2 twee valentie-elektronen. Alle atomen uit groep 13 hebben drie valentie-elektronen. De atomen uit groep 14 hebben vier valentie-elektronen enzovoort.
Voorbeeld: Zuurstof (O) heeft atoomnummer 8 en staat in periode 2 en groep 16 van het periodiek systeem. Het heeft dus 8 elektronen die verdeeld zijn over 2 schillen. Schil 1 bevat dan twee elektronen en schil 2 zes elektronen. Groep 16 heeft 6 valentie-elektronen. De zes elektronen in de tweede schil zijn bij zuurstof dan dus de valentie-elektronen, zuurstof kan dus zes bindingen aangaan met andere atomen.
Oefeningen
Het massagetal van een natriumatoom is 23. Het atoomnummer van natrium is 11. Hoeveel neutronen zitten er in de kern van een natriumatoom?
Koolstof (C) heeft atoomnummer 6 en staat in periode 2 en groep 14 van het periodiek systeem. Hoeveel schillen gebruikt koolstof en hoeveel valentie-elektronen heeft koolstof?
Leerlingen die hier vragen over hebben, keken ook naar:
Wat zijn atomen en waaruit bestaan ze?
Fasen: in welke toestanden kan een stof voorkomen en wat zijn de verschillen?
Werkt u in het vo of mbo? Plan direct een vrijblijvende demonstratie in!
We laten u graag geheel vrijblijvend zien hoe Mr. Chadd werkt, hoe het kan worden ingezet en wat de meerwaarde is. Dit doen we in een fysieke of online afspraak van zo'n 30 minuten. Let op! Deze demonstratie is alleen bedoeld voor mensen die werkzaam zijn in het vo of mbo, NIET voor leerlingen!

Meer informatie over Mr. Chadd
Laat hieronder uw gegevens achter en we sturen u geheel vrijblijvend meer informatie over Mr. Chadd op!

Werkt u in het vo of mbo? Neem contact op!
Bent u benieuwd naar de voordelen van Mr. Chadd of heeft u andere vragen? Laat uw gegevens achter en wij nemen zo snel mogelijk contact op.


